اسید سیتریک چیست؟
اسید سیتریک، یک ماده طبیعی و متابولیت متداول در گیاهان و حیوانات است. این اسید چند منظوره و پرکاربردترین اسید آلی در مواد غذایی، نوشیدنیها و داروها است.
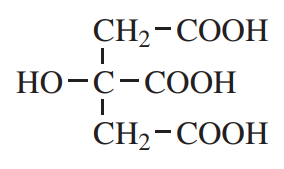
به دلیل عملکرد و قابلیتهای آن، اسید سیتریک و نمکهای آن (به ویژه سدیم و پتاسیم) در بسیاری از کاربردهای صنعتی برای کلاتهسازی، پایدار کردن pH، تنظیم pH و مشتق سازی استفاده میشوند. این استفادهها شامل مواردی مانند مواد شوینده لباس، شامپو، لوازم آرایشی، بازیابی نفت بهبود یافته و تمیزکردن شیمیایی میشود.
تاریخچه:
تاریخچه اسید سیتریک به زمان حدود 1200 میلادی بازمیگردد، زمانی که الکیمیست وینسنتیوس بلواکنسیس متوجه شد که شیره لیمو و نارنگی شامل یک ماده اسیدی است. در سال 1893، وهمر نشان داد که برخی از قارچها وقتی روی محلولهای قندی رشد میکنند، اسید سیتریک تولید میکنند. تولید اسید سیتریک نوع خمیری با استفاده از محیط کربوهیدراتی (شکری) تقریباً تنها روش تجاری برای تولید اسید سیتریک میباشد.
منابع طبیعی اسید سیتریک

اسید سیتریک به طور گسترده در گیاهان و حیوانات موجود است. این ماده بیشتر در میوههای گوناگون از جمله مرکبات وجود دارد، اما همچنین به صورت اسید آزاد یا نمک در میوهها، دانهها یا آبمیوههای متنوعی از گیاهان و گلها یافت میشود. همچنین، یون سیترات در تمام بافتها و مایعات حیوانی وجود دارد.
نقش فیزیولوژیکی اسید سیتریک در بدن
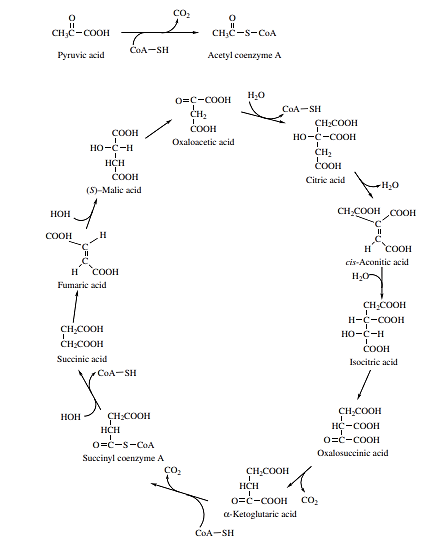
اسید سیتریک در انتهای سیسم متابولیسم اکسیداتیو تقریباً همهی موجودات تولید میشود. این سیستم متابولیسم اکسیداتیو (شکل 1)، به نام سیکل کربس ((Krebs cycle یا چرخه اسید سیتریک نامیده میشود. این چرخه، انرژی لازم برای رشد، حرکت، تولید مثل و غیره را فراهم میکند. بسیاری از مخمرها، قارچها و باکتریها چرخه اسید سیتریک را انجام میدهند و بر اساس میزان تولید اسید سیتریک، برای برآورده کردن اسید سیتریک مورد نیاز در فرایندهای تجاری انتخاب میشوند.
کاربردها
اسید سیتریک به دلیل ویژگیهای منحصر به فردی که دارد در بسیاری از صنایع غذایی و صنعتی استفاده میشود. از آن برای تنظیم اسیدیته (pH)، کنترل و حفظ pH (در محدوده 2.5 تا 6.5)، به عنوان یک کیلیت کننده برای ایجاد ترکیبات پایدار با یونهای فلزی چندتایی و به عنوان عامل پراکنش برای استحکام دادن به امولسیونها و سایر سیستمهای چندفازی استفاده میشود. به علاوه دارای طعم ترش و خوشمزه است که آن را به عنوان اسیدیته مورد علاقه در محصولات غذایی و نوشیدنی انتخاب میکنند.
1. کاربردهای غذایی
نوشیدنیها
اسید سیتریک، سدیم سیترات و پتاسیم سیترات به طور گسترده در نوشیدنیهای گازدار و بیگاز استفاده میشوند. حلالیت بالای اسید سیتریک در نوشیدنیها اهمیت دارد. اسید سیتریک همچنین با سایر اسیدها (مانند اسید مالیک) ترکیب میشود و به تولید طعم منحصر به فرد کمک میکند. میزان استفاده از اسید، به طعم مورد نظر در محصول و همچنین ارزیابی طعم و سلیقه مشتری وابسته است. اسید سیتریک و نمکهای سدیم و پتاسیم آن نیز برای استحکام pH در نوشیدنیهای کم کالری که شامل شیرین کنندههای حساس به اسید هستند، استفاده میشوند. غلظت اسید در بیشتر نوشابههای گازدار در محدوده 0.10 تا 0.25 درصد وزنی است.
اسید سیتریک و نمکهای سدیم و پتاسیم آن در مخلوطهای نوشیدنی خشک، چای کیسه ای، نوشیدنیهای نوآورانه و مخلوطهای کوکتل برای کنترل pH و ایجاد طعم استفاده میشوند. غلظت این اسید در طعمهای میوهای 0.10 تا 0.55 درصد است.
مربا، ژله
اسید سیتریک در مربا و ژلهها برای ایجاد طعم ترشی، تنظیم pH محصول و برای ژلهسازی بهینه استفاده میشود.
شیرینی و آبنبات
اسید سیتریک برای ترشی و ایجاد طعم ترش در آبنباتها اضافه میشود.
سالادها
ترکیبی از اسید سیتریک و اسید آسکوربیک، به جای سولفیت، در جلوگیری از قهوه ای شدن سبزیجات تازه استفاده میشود.
مواد غذایی نیمه پخته و منجمد
اسید سیتریک با ویژگیهای کیلیت کنندگی و اسیدی خود، باعث افزایش اثر آنتی اکسیدانها و غیرفعال کردن آنزیمهای طبیعی میشود و به پایداری محصولات غذایی نیمه پخته و منجمد کمک میکند. اسید سیتریک همچنین مانع تغییر رنگ و طعم میوههای منجمد میباشد.
کنسرو میوهها و سبزیجات
استفاده از اسید سیتریک برای تنظیم pH اسیدی (پایین تر از 4.6) میتواند نیازهای پردازش حرارتی را در میوهها و سبزیجات کنسرو شده کاهش دهد. علاوه بر آن، اسید سیتریک میتواند فعالیت اکسیداسیون و تغییر رنگ را کم کند و طعم، مخصوصاً میوههای کنسرو شده، را بهبود بخشد.
چربی و روغنها
از اکسیداسیون چربی و روغن در محصولات غذایی میتوان با استفاده از افزودن اسید سیتریک، جهت کیلیتسازی فلزاتی که کاتالیزور اکسیداسیون هستند، جلوگیری شود. علاوه بر این در فرآیند تصفیه روغن از اسید سیتریک برای حذف کلروفیل و فسفولیپیدها استفاده میشود.
شیرینی و دسرها
در صنعت شیرینی از اسید سیتریک و سدیم سیترات برای بهینه سازی خواص ژلسازی، ایجاد ترشی و بهبود طعم استفاده میشود. اسید سیتریک در محصولات شیره نباتی، قرص، آب نباتی و ژلهای مبتنی بر نشاسته به عنوان افزونه طعم استفاده میشود.
پنیر
در پنیرهای تصفیه شده و پنیر برش زده برای استحکام بافت پنیر، سدیم سیترات استفاده میشود. همچنین در تولید پنیر موزارلا به عنوان عامل کامل کننده استفاده میشود.
محصولات لبنی
سدیم سیترات نقش پایدار کننده مهمی در خامهزنی و جایگزینهای گیاهی لبنی دارد. اضافه کردن سدیم سیترات به بستنی، شیر و دسرهای منجمد قبل از پاستوریزاسیون و هموژنیزاسیون از ویسکوزیته مخلوط میکاهد و باعث میشود تا خامه راحتتر هم بخورد.
ماهی و محصولات دریایی
اسید سیتریک در ترکیب با سایر مواد نگهدارنده / آنتیاکسیدان، به کاهش pH و کنترل رشد میکروبهایی که منجر به فاسد شدن، تشکیل طعم غیرمطلوب و تغییر رنگ در ماهی و سایر محصولات دریایی میشود، کمک کند. همچنین از آن برای کیلیت کردن فلزات ردیف اول که در محصولات وجود دارد و واکنشهای اکسیداسیون را کاتالیز میکنند، استفاده میشود.
محصولات گوشتی
اسید سیتریک در محصولات گوشتی کیتوزنی برای افزایش کارایی مواد نگهدارنده و آنتیاکسیدان ها، استفاده میشود. از آن در محلولهای شستشوی گوشت برای تنظیم pH و افزایش خواص ضد میکروبی استفاده میشود. اسید سیتریک یا سدیم سیترات میتوانند جایگزین مناسبی به جای ۵۰٪ از شتابدهندههای نگهدارنده نظیر اسید آسکوربیک، اریتوربیک، سدیم آسکوربات و سدیم اریتوربات باشند.
2. کاربردهای دارویی
سیتریک اسید و نمکهای سیترات در صنعت داروسازی به عنوان خنثی کنندهی pH به کار میروند. به کمک این اسید و نمکها، محصولات دارویی میتوانند در pH بهینه خود قرار بگیرند و در نتیجه پایداری و اثربخشی بهتری داشته باشند. از اسید سیتریک و بیکربنات برای تسریع انحلال ترکیبات فعال و بهبود طعم دارو استفاده میشود. همچنین سیتراتها میتوانند با کیلیت کردن یونهای فلزی باعث جلوگیری از تجزیه و فساد دارو شوند. سیتراتها از انعقاد خون در پلاسما و قسمتهای مختلف جلوگیری میکنند. علاوه بر این، سیتراتهای کلسیم و سیترات آمونیوم آهن به عنوان مکمل معدنی استفاده میشوند. همچنین سیتریک اسید و فلوراید به عنوان مکمل در خمیر دندانها استفاده میشوند.
3. کاربردهای کشاورزی و دامپروری
سیتریک اسید و نمکهای آمونیوم آن در کودهای مایع به عنوان کیلیتهای محلول برای عناصر مغذی آهن، مس، منیزیم، منگنز و روی استفاده میشوند. همچنین در تغذیه حیوانات، این مواد به عنوان کیلیت قابل هضم برای عناصر غذایی فلزی مورد نیاز حیوانات استفاده میشوند.
4. کاربرد در صنایع دیگر
در زمینه شویندهها، نمک سدیم سیترات به عنوان یک ماده افزودنی برای شامپوها و شویندههای مایع استفاده میشود. در بسیاری از موارد سیتراتها جایگزین مناسب و دوستدار محیط زیست برای فسفاتها به شمار میروند. سیتراتها یونهای سختی آب را کیلیت میکنند. حلالیت بالا در آب و بهبود عملکرد شوینده در دما و pHهای خیلی پایین و بالا، کلید استفاده از سیترات در شویندهها است.
در محصولات شستشوی سطوح سخت، سیتریک اسید و سدیم سیترات به عنوان عاملهای اسیدی و کیلیت کننده به کار میروند تا آهک سخت آب را حذف کنند. در تمیزکردن فرشها، سیتریک اسید رنگدانهها را پایدار میکند و به ویژه در فرشهای مقاوم در برابر لکه، زردشدگی را از بین میبرد.
در تمیزکردن غشاءهای اسمز معکوس، از محلولهای سیتریک اسید برای حذف آهن، کلسیم و دیگر یونها استفاده میشود. محلولهای سیتریک اسید میتوانند این یونها را حل و حذف کنند بدون اینکه به غشاءها آسیب برسانند.
در صنعت ساختمان، سیتریک اسید و نمکهای سیترات به عنوان افزودنی در فرمولاسیون بتن، ملات و گچ استفاده میشوند تا زمان تنظیم (تنش و زمان لازم برای سفت شدن بتن) را کاهش دهند و مقدار آب مورد نیاز برای تهیه مخلوط را کاهش دهند. یون سیترات فرایند هیدراتاسیون سیمان پورتلند را کند میکند. در سطح کمتر از 0.1٪، سیتراتها باعث شتاب دادن به سرعت فرآیند میشوند، در حالی که در سطح 0.2-0.4٪ سرعت تنظیم بتن را کند میکنند. سیترات موجب افزایش مقاومت در دمای بالا و بهبود مقاومت در برابر یخ زدگی بتن و ملات میشود.
در صنعت نساجی، سیتریک اسید به عنوان یک بافر در تولید رزینهای گلیوکسال استفاده میشود که برای ماندگاری پارچهها مورد استفاده قرار می گیرد. همچنین، گزارش شده است که سیتریک اسید خصوصیت جدا شدن خاک را در پارچههای پنبه ای ضد چروک افزایش میدهد و در عملیات رنگرزی به عنوان یک بافر، کیلیت کننده و عاملهای اسیدی non-volatile تنظیم کننده pH استفاده میشود.
در صنعت پلاستیک، سیتریک اسید و بیکربنات به عنوان عامل دمش جوشانی به جای کلرید فلوروکربنها برای تولید ظروف غذا و نوشیدنی استفاده میشود. همچنین، سیتریک اسید به عنوان یک عامل کیلیت کننده در سیستمهای کاتالیزوری ساخت رزینها استفاده میشود و استرهای سیترات در فیلم PVC به عنوان ماده نرم کننده، به خصوص در بسته بندی محصولات غذایی، استفاده میشوند.
در صنعت کاغذ قبل از فرایند سفیدکردن، سیتریک اسید به سلولوز اضافه میشود تا یونهای فلزی را جدا و از تغییر رنگ جلوگیری کند. در کاغذ سیگار، سیتراتها برای کنترل سرعت سوختن در مقایسه با دخانیات استفاده میشوند.
خواص فیزیکی
اسید سیتریک بیآب، از محلولهای گرم آبی و به صورت بلورهای بیرنگ و شفاف یا پودر سفید بلوری تهیه میشود. برخی از خواص فیزیکی آن در جدول 1 آورده شدهاند. حلالیت اسید سیتریک در آب و برخی از حلالهای آلی در جدول 2 آورده شده است. pH و گرانروی ویژه محلول آبی اسید سیتریک نیز در جدول 3 نشان داده شده است.

جدول 1: خواص فیزیکی اسید سیتریک خشک
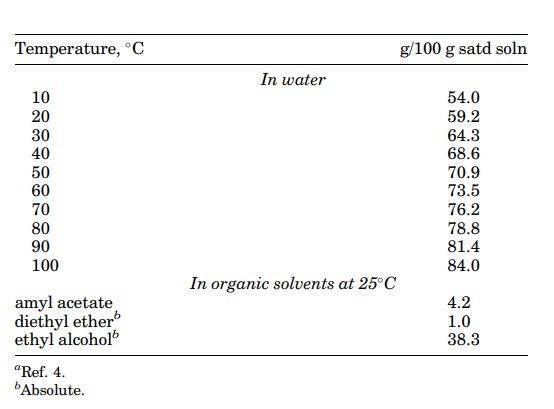
جدول 2: حلالیت اسید سیتریک خشک
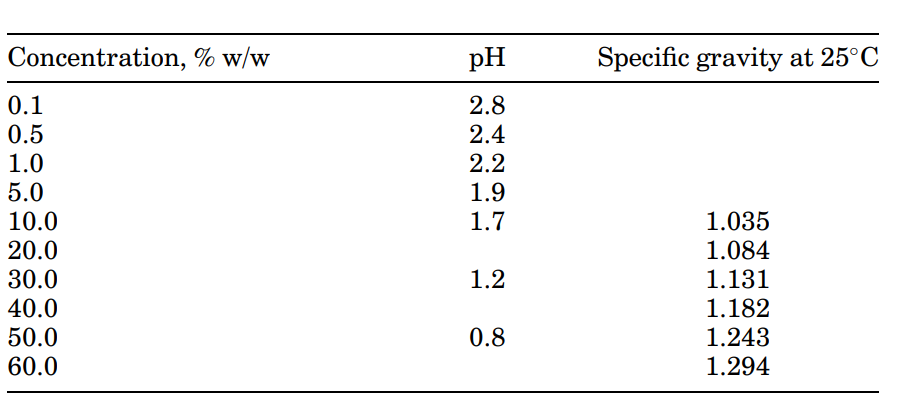
جدول 3: pH و گرانروی ویژه محلول آبی اسید سیتریک
محلولهای آبی اسید سیتریک، سیستمهای بافری تشکیل میدهند زیرا اسید سیتریک اسیدی ضعیف و سه گروه کربوکسیلی دارد. در 20 درجه سلسیوس، pK1 برابر 3.14، pK2 برابر 4.77 و pK3 برابر 6.39 است. محدوده بافر برای محلولهای سیترات pH 2.5 تا 6.5 است. بافرها میتوانند با استفاده از محلول اسید سیتریک و سیترات سدیم و یا با افزودن بازی مانند هیدروکسید سدیم تهیه شوند. جدول 4 pH محلولهای بافری که از ترکیب محلول قوی 0.1 M (0.33 N) اسید سیتریک با سیترات سدیم 0.1 M (0.33 N) بدست آمده را نشان میدهد.
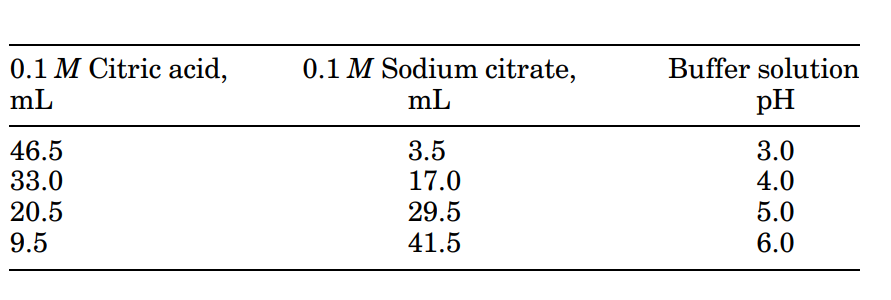
جدول 4: محلولهای بافری اسید سیتریک
اسید سیتریک مونوهیدرات وزن مولکولی 210.14 دارد و بلور آن از محلولهای سرد آبی تشکیل میشود. هنگامی که به آرامی گرم میشود، در دمای 70-75 درجه سلسیوس بلورها آب خود را از دست میدهند و در بازهی 135-152 درجه سلسیوس ذوب میشوند.
گرمایش سریع باعث میشود تا در دمای 100 درجه سلسیوس دهیدراته شود و بلورهایی با نقطه ذوب در 153 درجه سلسیوس تشکیل دهد. سیتریک اسید مونوهیدرات در مقادیر تجاری محدودی در دسترس است زیرا بیشتر مصرف کنندگان نیاز به فرم بیآب دارند.
خواص شیمیایی
اسید سیتریک اکثر واکنشهای هیدروکسی پلیکربوکسیلاتهای آلی مانند استرزایی، تشکیل نمکها و واکنشهای آنیدریدی را انجام میدهند. گروه هیدروکسیل در این ترکیب از نوع tertiary hydroxyl group بوده و به همین دلیل بعضی از واکنشها امکان پذیر نمیباشد.
1. تشکیل نمک
اسید سیتریک با بسیاری از کاتیونها مانند قلیاها، آمونیاک و آمینها نمکهای یک بازی، دو بازی و سه بازی تشکیل میدهد. نمکها میتوانند با خنثی کردن محلول اسید سیتریک در آب و یا با استفاده از باز مناسب و یا از تجزیه دو مرحلهای توسط یک نمک سیترات و یک نمک فلز انحلال پذیر تهیه شوند.
تری سدیم سیترات نسبت به سایر نمکهای اسید سیتریک بیشتر استفاده میشود و معمولاً با خنثی کردن یک محلول آبی از اسید سیتریک با استفاده از سدیم هیدروکسید تهیه میشود. این واکنش بسیار گرمازا است و انرژی J1109 به ازای هر گرم از اسید سیتریک تولید میکند. برای صرفه جویی در انرژی، حرارت تولید شده میتواند در مراحل غلظت و بلورسازی سدیم سیترات استفاده شود. منابع دیگری از یون سدیم که برای تهیه سدیم سیترات استفاده میشوند، سدیم کربنات و سدیم بیکربنات هستند. این واکنشها مقادیر زیادی گاز دی اکسید کربن تولید میکنند که منجر به تولید کف زیاد ولی گرمای کمتر میشود.
نمکهای مونوسدیم و دی سدیم سیترات با محدود کردن مقدار سدیم موجود در واکنش تولید میشود، به صورتی که یک مول از باز به ازای هر مول اسید سیتریک برای تولید مونوسدیم سیترات و دو مول از باز به ازای هر مول از اسید سیتریک برای تولید دی سدیم سیترات استفاده میشود. نمکهای تجاری دیگر اسید سیتریک در جدول 5 نشان داده شدهاند.
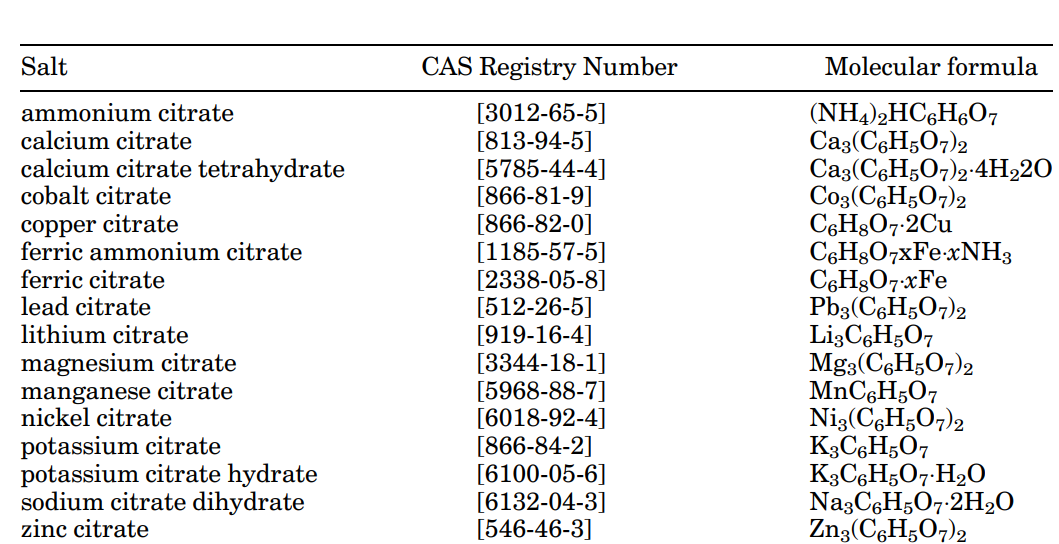
جدول 5: نمکهای اسید سیتریک
2. تشکیل کیلیت
اسید سیتریک با بسیاری از یونهای فلزی چندگانه مختلف برای تشکیل کیلیت واکنش میدهد. این ویژگی شیمیایی مهم باعث میشود که اسید سیتریک و سیتراتها در کنترل آلودگی فلزات چندگانه که میتواند رنگ، پایداری یا ظاهر یک محصول یا کارایی یک فرآیند را تحت تأثیر قرار دهد، مفید باشد.
اسید سیتریک با گروه هیدروکسیل و سه گروه کربوکسیلی خود، لیگاند چند دندانه میسازد. دو یا بیشتر از این گروهها برای تشکیل ساختار حلقوی استفاده میشوند. نسبت مولی عادی فلز به لیگاند 1: 1 است. با برخی از یونهای فلزی، در شرایط خاص، ممکن است بیش از یک حلقه تشکیل شود که نسبت فلز به لیگاند بیشتری را ممکن میکند.
وقتی یک یون فلزی با یک لیگاند مانند اسید سیتریک کیلیت شود، دیگر آزاد نیست تا واکنشهای شیمیایی خود را انجام دهد. یک یون فلزی که به طور معمول رنگدار است، ممکن است در حضور سیترات، رنگ کمتری داشته باشد و یا اصلا هیچ رنگی نداشته باشد. مولکولهای آلی که در حضور یونهای فلزی کاتالیزور تجزیه میشوند، با کیلیت کردن یونهای فلزی با اسید سیتریک پایدار میشوند.
کیلیت یک واکنش تعادلی است. همواره برخی از یونهای فلزی آزاد همراه با یونهای فلزی کیلیت شده وجود دارند. تابع لگاریتم نسبت یونهای فلزی کیلیت شده به یونهای فلزی آزاد به عنوان ثابت پایداری یا ثابت تشکیل نشان داده میشود که در جدول 6 نشان داده شده است. هر چه ثابت پایداری بالاتر باشد، درصد بیشتری از یونهای فلزی کیلیت شده است. ثابتهای پایداری در pH بهینه خود اندازهگیری میشوند. به طور کلی، ثابتهای پایداری برای سیتراتهای فلزی در pH کمتر از 2-3 بسیار کم، در pH 3-10 بالا و در pH بالاتر از 10-12 کم است.
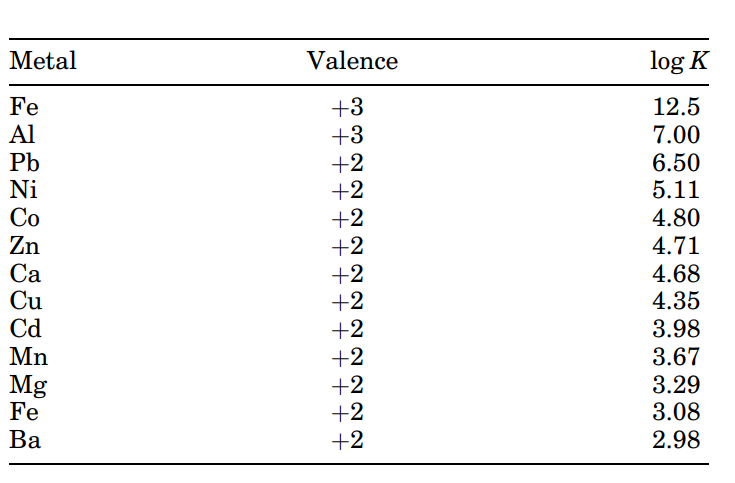
جدول 6: ثابت پایداری برای سیترات فلزها
حمل و نقل و نگهداری
اسید سیتریک خشک، بدون بروز مشکل میتواند به صورت خشک ذخیره شود، با این حال باید از نگهداری در شرایط رطوبت بالا و دمای بالا خودداری کرد تا از تشکیل گچ جلوگیری شود. ذخیره سازی باید در ظروف محکم صورت گیرد تا از تماس با هوای مرطوب جلوگیری شود.
اسید سیتریک مایع به صورت تجاری در انواع غلظتها، خلوص و رنگ وجود دارد. اسید سیتریک مایع باید در دمای بالای صفر درجه سانتیگراد نگهداری شود تا از تشکیل بلور جلوگیری به عمل آید.
محلولهای اسید سیتریک برای بتن معمولی، آلومینیوم، فولاد کربن، مس و آلیاژهای مس خورنده هستند و نباید با نایلون، پلی کربنات، پلی آمیدها یا آکریلیکها استفاده شوند.
قیمت و خرید اسید سیتریک آبدار
برای سفارش اسید سیتریک آبدار (اسید سیتریک مونوهیدرات) با مناسبترین قیمت، با شمارههای زیر تماس بگیرید:




















